导语:寨卡病毒肆虐,令人头疼不已,防治蚊子传播病毒确实势在必行,但是如何战胜这些蚊子呢?众所周知,如今修改基因技术发展迅速,那么转基因技术必不可少么……
关键词:蚊子,病毒传播,基因修改,人工选择
近来寨卡病毒肆虐,使得人类恐慌连连。与此同时,还引发了新的问题,亟待解决——即如何最有效地控制这些传播人类疾病的蚊子。如今在全球范围内,埃及伊蚊叮咬人体后,会传播三种病毒性疾病:登革热(dengue)、基孔肯雅(chikungunya)和寨卡(Zika)。而且我们一旦感染这些病毒,目前尚未研发出有效的疫苗或者具体的药物可以治疗。
目前,控制蚊子数量是限制其传播病毒的唯一方法,但这绝非易事。而且我们以往的控制方法如今已不再实用,比如使用杀虫剂。因为杀虫剂会对环境造成不良影响,同时还会增强残留蚊群的抗药性。所以现在,控制蚊子的新方法迫在眉睫。
因此,传病媒介生物学家们长久以来的梦想(我也是其中一员)终于有机会得以实现:即通过修改基因来阻止或限制蚊子传播疾病。在过去几十年间,虽然基因编辑技术发展迅速,但我认为我们还是忽略了那些更加传统的,对这些昆虫行之有效的可靠方法。正如几百年来,针对其它植物和动物所采用的选择性培育技术一样,如今我们也可以通过培育不能传播人类病原体的蚊子来达到这个目的。

在巴西的坎皮纳斯,来自Oxitec检查的技术人员对埃及伊蚊进行了基因修改。图片来源:Paulo Whitaker/Reuters
公开的技术
事实上,有一个经典策略可以减少昆虫数量——通过放射性照射来培育一大批不育的雄性昆虫。当目标昆虫群中的雌性与这些雄性交配,则无法产生可育的后代——故以此来大大减少其数量。
现代对这种方法的改进之处在于:这些培育的转基因雄性昆虫都携带着一个使其不育的显性致命基因,导致其后代在幼虫期死亡,所以其后代得以消除。这种方法也得到了Oxitec 生物科技公司的青睐,而且最近已在巴西投入使用。
其实,我们不仅仅是要杀死这些蚊子,而是需要一个更持续有效的策略,即修改基因使其无法再传播疾病细菌。
新的CRISPR基因编辑技术使转基因取代野生种群的基因。这种方法不仅在蚊子当中效果显著,而且是一种“驱动”转基因扩散到野生蚊群中的潜在方式。CRISPR技术有助于快速传播这种基因,而这种基因能够阻止蚊子传播病毒——科学家们将其称作不应性(refractoriness)。
但是CRISPR技术也颇具争议,尤其将其运用到人类自身时,因为植入个体的转基因可以遗传到下一代。毫无疑问,采用这种技术培育修改基因的蚊子,并释放到自然界中,势必会引发广泛辩论。对此,美国国家情报局局长James Clapper就把这种技术称为潜在的大规模杀伤性武器。
但是,转基因技术对于修改基因的蚊子来说真的必不可少么?
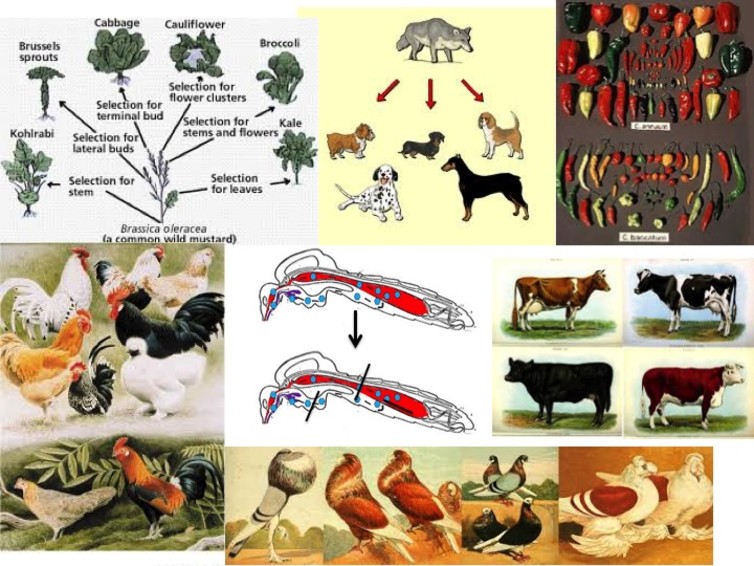
如图所示,这是这些年间人工选种的成功案例。图中心位置是一个科学家们为蚊子量身定做的“障碍”,这样一来它们就无法传播病毒。图片来源:Jeff Powell, Author provided
老办法——选择育种
几百年来,我们在修改基因以控制种族数量方面已取得卓越成效。而且这已经运用到几乎所有具有商业价值的植物和动物身上。而这些植物和动物可供人类食用或者作其他用途,包括棉花和羊毛。的确,选择育种可以自发产生许多不同的变体。
尤其在农业领域中,利用这种自然变体的人工育种更是屡试不爽。在连续几代中,通过选择优良性状的亲代(比如产蛋量更高的母鸡和羊毛更软的绵羊),就会产生一个“真实遗传”(true-breeding,是指子代性状永远与亲代性状相同的遗传方式,或生物性状能够代代相传、稳定遗传),这样就可以一直保持这种所需性状。这些子代可能与其祖先迥然不同,比如狼族祖先发展而来的所有狗的品种,也是各式各样。
到目前为止,虽然我们在蚊子身上所进行的这类实验非常有限,但这些有限的实验也表明,我们有可能选育出疾病传播能力较弱的蚊子。因此,与其从其它物种人工植入转基因,为何不直接利用蚊群的自然遗传变异呢?
通过人工选育的蚊子变体与转基因蚊子相比,有以下几个优势。
首先,如果采用人工选育,所有关于转基因生物(GMOs)的争议与潜在威胁都可以避免。我们只需要关心,在自然产生的基因变异的蚊子中,携带着我们所选基因的蚊子总数量增多。
其次,人工选育的蚊子直接来自于目标蚊群,将其释放到野外会更具有竞争力。因为这些新的有不应性特征的变体所携带的无法传播病毒的基因均来源于目标蚊群,所以它们能更好地适应当地环境。而众所周知,实验室所培育的转基因蚊子适应性则较差。
再者,人工选育能因地制宜。科学家们可以从当地的蚊群着手,就在本地及时地,针对性地选择抵抗时下感染人类的一些顽固性病毒的不应性基因(refractoriness)。比如按血清分类,登革病毒有四种的不同“变形”模式。要控制该疾病,所选择的蚊子必须对当前肆虐的类型有抗性。
另外,人工选育也可能选出不能传播多种疾病的蚊子变体,因为只要相同的埃及伊蚊蚊种传播登革热(dengue)、基孔肯雅(chikungunya)和齐卡病毒(Zika),那么我们居住在有这些蚊子环绕的地方,就同时有感染这三种病毒的威胁。虽然这一说法尚未得到证实,但同样没有理由否定:精心设计的人工选种可以培养出不能传播所有病毒的蚊子。
幸运的是,埃及伊蚊最容易圈养,而且培育一代只需每两周半。所以不像那些传统的植物或是动物选种,培育一代需要数年,蚊子十代的选种只需短短几个月。

研究人员正在研发大批量的埃及伊蚊圈养技术——(它们)培育一代蚊子只需两周半周。来源:IAEA Imagebank, CC BY-NC-ND
但这不意味着采用这种人工选育的技术就一帆风顺,毫无障碍。也许最关键之处在于:与野生蚊群相比,使这些蚊子难以传播疾病的基因也会让其体质变弱、生存力降低。最终,实验室培育的蚊子与其后代就会失去竞争力,并逐渐在野生蚊群中消失。我们可能需要不间断地释放培育的蚊子——即疾病传播能力较弱的蚊子——来与野外身强力壮的蚊子竞争。
更糟糕的是,蚊子所携带的病原体本身还会发生变异。而病毒变异就可能躲过修改基因的蚊子的阻挡。所以为预防病毒或者其它病原体发生变异,任何针对修改基因的蚊子的计划都应该有“应急计划”。这样,我们可以迅速选出新的蚊子变体来对抗新版病毒——而无需依赖高额的转基因技术。
如今,在种植植物和饲养动物方面,为了进一步改善某些商业价值高的物种,我们越来越多地用到新的基因操作技术。但这仅仅用在传统的人工选育尽可能地改善其品种之后。对此,目前许多研究蚊子的生物学家建议直接采用最新的转基因方法,而这些转基因在野生的蚊群中从未证实过是有效的。他们实际上是跳过了一个已经证实的、低成本而且争议更少的方法,而这种办法至少值得我们一试。
作者:Jeffrey Powell,耶鲁大学教授。
(翻译 夏雪)
(审校:张玲)
原文链接【科学美国人博客】:
https://theconversation.com/to-fight-zika-lets-genetically-modify-mosquitoes-the-old-fashioned-way-57789


















留言