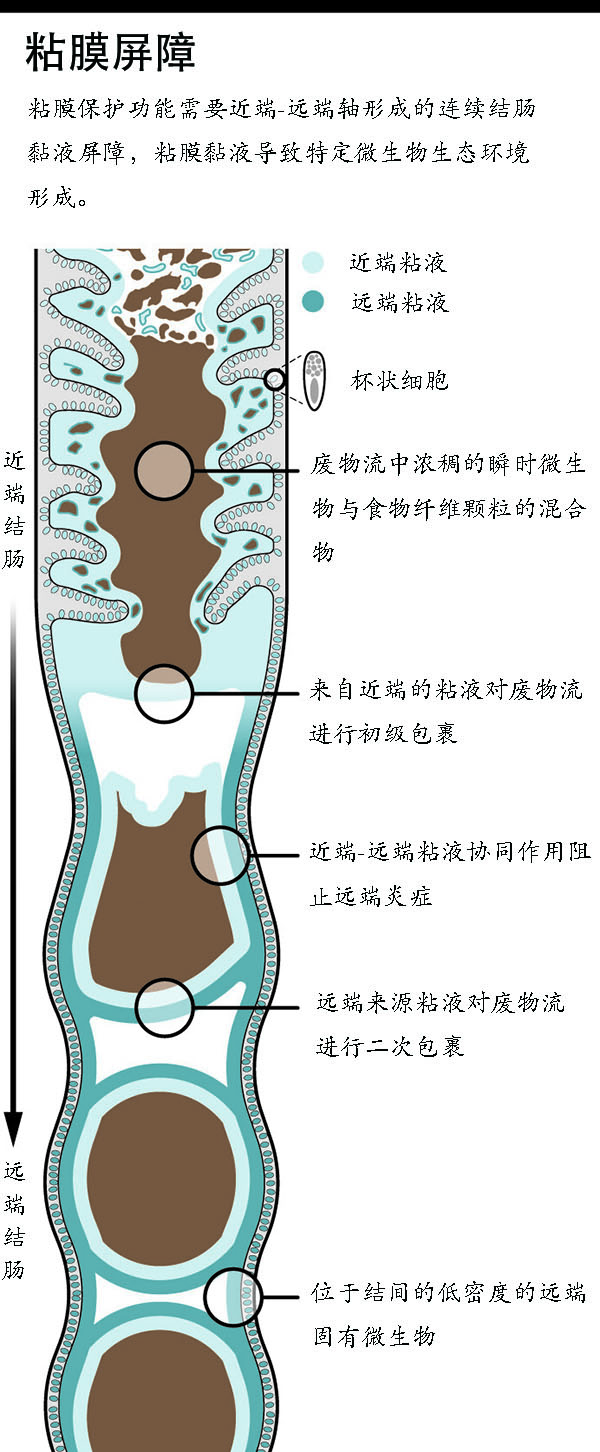
新发现重塑肠道菌群理论。图片描述了黏膜屏障的形成。 图片来源:Val Altounian/AAAS
微生物居住在人类肠道,是我们细胞数量的10倍以上。如今,奥克拉荷马医学研究基金会(Oklahoma Medical Research Foundation,OMRF)的科学家有了新发现,重新定义所谓的肠道菌群如何运作,以及我们的身体如何与100万亿肠道细菌共存。
这项新研究发表在《科学》(Science)杂志上,有望为炎症性肠病以及因结肠癌和溃疡性结肠炎等疾病而切除部分肠道的患者提供新的治疗方法。新发现也将有助于阐明,为何使用抗生素会引起消化系统各方面的问题。
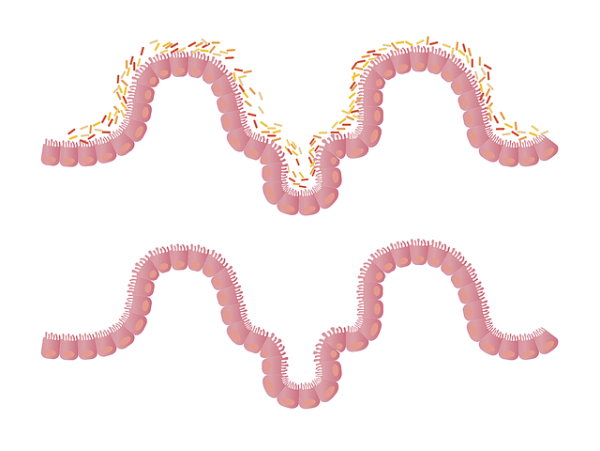
图片来源:Pixabay
由OMRF的医学和哲学博士Lijun Xia领导的科学家团队,通过研究模型发现微生物群控制着一种黏液层的形成,黏液富含糖分,包裹粪便物并随之移动。研究人员的发现与先前设想不同,黏液作为屏障,隔开粪便中的细菌和结肠中成千上万的免疫细胞。一旦失去黏液,整个系统将完全失衡。
OMRF生物医学研究的Merrick基金负责人Xia说:“结肠不仅仅是一个消化器官,还是一个免疫器官。我们的微生物群自我们出生时就开始发展,它的进化贯穿我们一生。这对我们体内获得性免疫系统的成长和成熟很重要。如果免疫系统发育不良或没有得到良好的护理,它就不能正常运转,就可能导致疾病。”
肠道微生物群的整体健康有赖于黏液的存在。尽管黏液的产生会受到干扰,但是OMRF的研究人员发现,黏液分泌可以恢复。
研究过程中,研究人员发现,使用广谱抗生素处理小鼠后,粪便物没有丝毫的黏液包裹。在接受粪便物微生物组移植后,失去黏液保护的小鼠重新出现黏液分泌的增长。
Xia解释说,这对微生物群失衡的患者有显著的治疗意义。
Xia说:“无论是因为抗生素干扰黏液形成,或是溃疡性结肠炎后切除所有的结肠,这都会引起痛苦的炎症反应。如今我们更清楚黏液的作用和起源,我们还会研究该如何使用或恢复它的产生。”
OMRF主席Stephen Prescott医学博士强调,随着科学家意识到肠道微生物对我们整体健康的作用,它在医学研究中越发受到重视。

OMRF科学家Lijun Xia,医学和哲学博士。 图片来源:OMRF
Prescott说:“研究人员发现,这些生活在我们消化道的微生物,可能在肥胖、糖尿病和各种自身免疫以及消化疾病中扮演重要角色。Xia博士的成果证实,微生物群产生的保护黏膜和疾病发展(如结肠炎等)存在很强的关系。”
这项研究可能会打开新的大门,改变使用结肠镜监测疾病(如炎症性肠炎)的手段。Xia说:“相比于重复使用侵入性手段跟踪炎症性肠病,我们可通过检测粪便样本中黏液的存在情况,评估病人的肠道是否健康。”
Prescott补充说,研究的结果影响深远,并强化了“基础”科学的重要性。
Prescott说:“我们的研究人员要明晰这种黏液的起源和功能,以及它与微生物群有什么关联,进而研究它与疾病的关系。我们现在明白,如果肠道微生物和黏液失衡,长期健康问题可能会很严重,而Xia博士的工作可以帮我们找到答案。”
翻译:陈振翀
审校:巢栩嘉
引进来源:奥克拉荷马医学研究基金会


















 京公网安备11010502039775号
京公网安备11010502039775号





