肿瘤治疗现状与展望
2021-10-22 10:56:00肿瘤是影响人类健康的重要疾病,现已成为全球第二大死亡原因。肿瘤治疗主要包括传统的手术治疗、放射治疗、化学治疗和近年来发展迅速的靶向治疗、免疫治疗等新型治疗方式。
随着肿瘤分子生物学与基因组学的发展,人们对肿瘤分子表型的认识也不断加深,肿瘤治疗的策略从既往围绕发病部位和形态病理为核心的系统化疗阶段,逐渐转变为针对驱动基因突变的精准靶向治疗时代。肿瘤靶向治疗即通过特异性靶向在肿瘤发生和进展中发挥重要作用的分子或信号通路,对肿瘤进行治疗的方法。基于肿瘤特定分子表型给予相应的靶向治疗已成为当前晚期肿瘤治疗的首选方案。
靶向药物一直是抗肿瘤药物研发的热点。肿瘤靶向药物大体可分为单克隆抗体和小分子化合物两大类。近年来随着研究的深入,新靶点不断涌现,抗肿瘤药物研发取得了很多突破性进展,肿瘤靶向药物以每年5~6个的速度不断增加。截至目前,美国食品药品监督管理局(FDA)已批准了针对30余种靶点的肿瘤靶向治疗药物,其中很多都获批治疗多个适应证,这些药物的出现为肿瘤患者带来了新的希望。
全基因组测序、靶向高通量测序和深度测序等技术的进步为异常肿瘤基因的检测带来了突破。高通量测序能确定肿瘤中所有类别的基因组改变,这些测序结果为肿瘤患者个性化靶向药物的选择提供了重要依据。然而,目前的临床数据表明,仅有约15%的肿瘤患者可根据测序结果选择相应的、已上市的靶向药物,10%左右的肿瘤患者可用的靶向药物还处于临床试验中,另有10%~15%的患者可用的靶向药物仅处于动物实验阶段。在新的肿瘤基因组学等多组学技术支持下,2014年美国癌症研究学会(AACR)提出了一类创新性临床试验——“篮子试验”(Basket Trial),即将针对某一特定靶点的药物作为篮子,将有相同分子事件的不同肿瘤放入该篮子进行研究。“篮子试验”使肿瘤治疗不再被传统的解剖部位或病理类型所限制,而是加入了肿瘤基因遗传背景与分子分型,有望推动肿瘤,尤其是难治性肿瘤的精准诊疗。
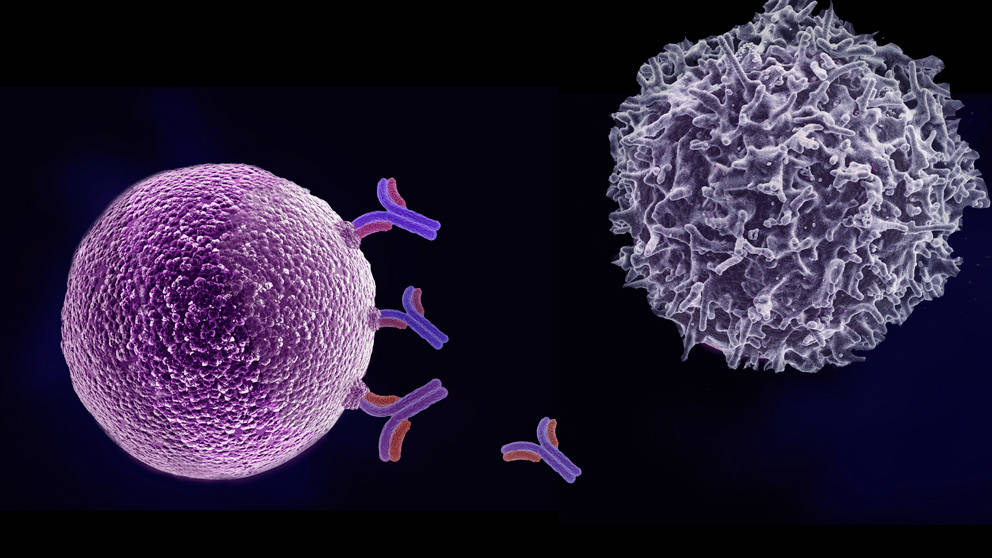
肿瘤免疫治疗主要是应用免疫学原理和方法,激发和增强机体抗肿瘤免疫应答,杀伤肿瘤细胞,抑制肿瘤生长,如嵌合抗原受体(CAR)治疗和靶向程序化死亡受体1(PD-1)治疗等。肿瘤免疫疗法与传统的化疗和放疗相比,具有疗效显著、效果持久和毒副作用小等优势。目前,PD-1/PD-L1抗体药物已被批准用于恶性黑色素瘤、非小细胞肺癌、肾癌、膀胱癌、头颈部鳞癌等肿瘤以及所有微卫星不稳定的实体瘤,是近年来肿瘤治疗领域的重大进展。2018年8月,靶向PD-1/PD-L1的免疫治疗药物正式进入中国市场,为对传统治疗无效的肿瘤患者提供了全新的治疗方案。然而,临床试验表明,仅有20%~40%的患者能从PD-1免疫疗法中获益,许多免疫原性不足或肿瘤内缺乏免疫细胞浸润的实体瘤都对PD-1治疗无应答。
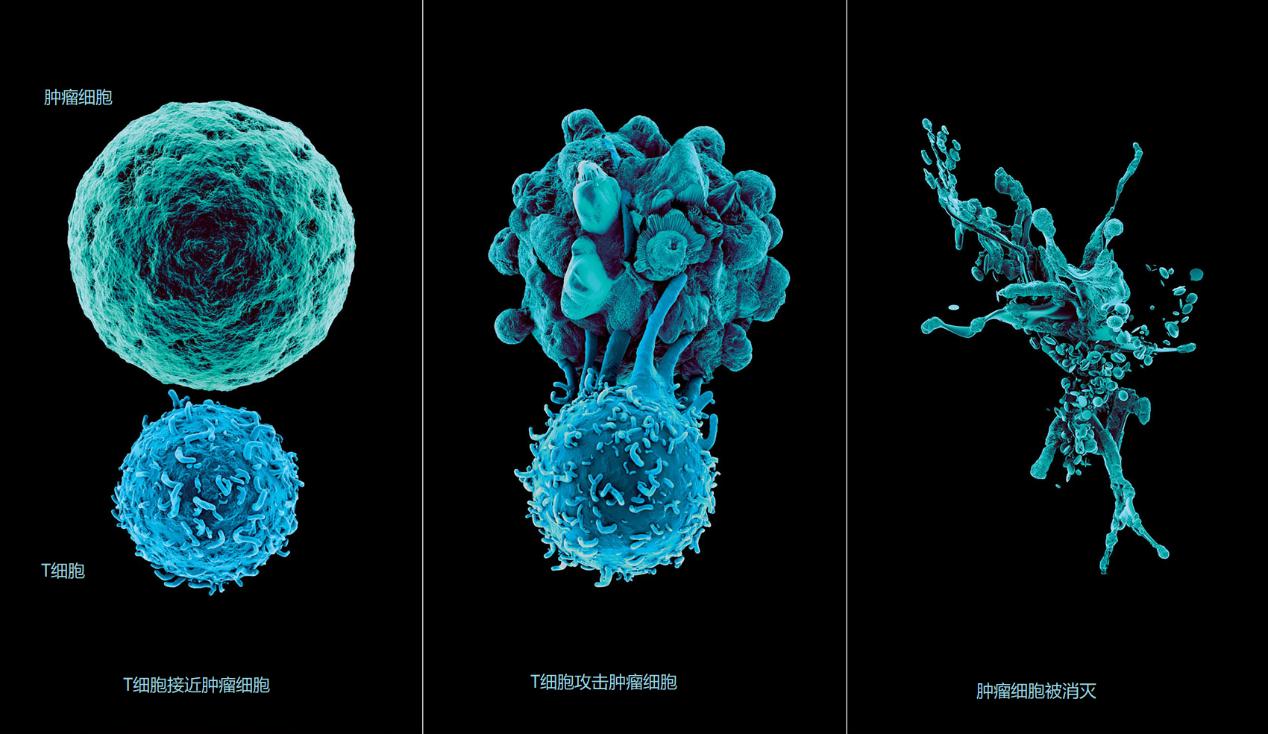
过去的几十年里,尽管肿瘤靶向治疗和免疫治疗等新型疗法都取得了许多突破,但其在肿瘤精准诊疗中还存在许多局限性。作为肿瘤进化的核心事件,肿瘤异质性和动态性的特征为肿瘤治疗带来了严峻挑战。同时,肿瘤与微环境间的相互作用和动态变化让肿瘤治疗更为复杂和艰巨。如何检测不同肿瘤的异质性,如何筛选对特定药物敏感的个体,如何克服患者对靶向药物的耐药性,如何有效评估和监测疗效,如何将靶向药物与常规疗法或免疫疗法相结合,都是亟待解决的问题。液体活检、大数据、人工智能等新方法、新技术的出现为肿瘤诊疗提供了新的工具和支撑,使多途径、多靶点、多时空的干预方式成为可能,也将使得抗肿瘤治疗更为精准,疗效更好。
王红阳,肿瘤学、分子生物学专家,中国工程院院士,发展中国家科学院院士,教育部长江特聘教授,主任医师,博士生导师,国家杰出青年基金获得者。现任国家肝癌科学中心主任,国际合作生物信号转导研究中心主任。兼任中国抗癌协会副理事长,中国医师协会精准医学专业委员会主任委员,上海市医学会副会长。
本文来自《张江科技评论》












 京公网安备11010502039775号
京公网安备11010502039775号





