让已经陷入生命危险的病患使用未经批准的药物,只会带来虚假的希望。图片来源:pixabay
毫无疑问,美国这个新的法案听起来很棒。特朗普总统对营销有那么点了解,他5月30日签署“尝试权”法案时,一直在滔滔不绝地谈论着这个法案的名字。他被身患不治之症的患者包围,其中包括一位患有杜氏肌营养不良的二年级小学生。这位患者从自己的小轮椅里站起来,拥抱了总统。出台法案,是想让这样的患者能绕过美国食品及药品管理局(FDA),更容易地使用试验中的药物。
这项法案的名字和概念都非常讨喜,美国已经有40个州通过了类似的法规,不过在联邦政府加入进来之前,那些法规基本是象征性的。各州的法规不尽相同,大体意思都是,临终患者可以向制药厂商寻求任何已经通过I期临床试验的药物(I期试验只是最小型的安全试验)。“我们将会拯救大量生命,”特朗普说,“目前FDA的审批流程可能要花很多很多年,患者却没那么多时间。”
深入了解以后,你会发现将FDA视为障碍是不对的,这项法案也不像宣称的那么美妙。“这应该叫询问权,而不是尝试权。”纽约大学的医学伦理学家艾莉森·贝特曼-豪斯(Alison Bateman-House)说,她赞同同情性地使用试验药物。而对这类药物的询问权本来就存在。她说:“如果我有魔法,就会想办法让患者知道已经存在的项目,而不是通过一项让人感觉良好的法案。”
事实上,几十年来制药公司一直通过FDA监管的项目,让患者可以接触未经批准的药物。这种“扩大使用”(expanded access,也叫“同情使用”)的目标患者,是部分不符合正式药物研究要求而没法参与试验的重病患者。根据2016年的报道,FDA每年会收到1000多份代表这类患者的申请,其中99.7%都会得到批准。据FDA局长斯科特·戈特利布(Scott Gottlieb)说,在紧急情况下,申请会立即被批准,一般的批准周期也只有几天。

图片来源:pixabay
但是,这些可能无效或不安全的药物,存在使用障碍。有些患者找不到愿意管理他们用药的医生,或找不到可以提供场所让他们使用药物的机构,还有很多药物根本就拿不到。你无法强迫制药厂商做这件事:2007年,美国联邦法院的一项裁决认为,“并不存在让末期疾病患者使用试验药物……的基本权利”。新的法案丝毫没有改变这一点。
制药公司也有很多理由对此保持谨慎。处于早期试验阶段的药物,风险和收益都存在很大的不确定性。产量可能有限,生产成本又高,公司通常希望节约珍贵的库存做临床试验。研发人员也担心,他们的药在虚弱的临终患者身上可能会效果不佳。一旦消息传出去,又会造成悲剧:患者会被吓得不敢参与研究,投资者会撤资,股票会下跌。有潜在价值的新药研发工作,很有可能因为出于同情偏离正轨。
“假如患者可以抓起电话就说‘我需要药,把药给我’,怎么还会有人去做临床试验?”匹兹堡“认知疗法”(Cognition Therapeutics)公司总裁、CEO肯尼思·莫克(Kenneth Moch)问,“以后的患者会怎么样?”他怀疑制药行业不会接受“尝试权”,并在一次关于该法案的国会听证会上说:“任何一个我认识的遵守伦理的药物开发者,都不会允许药物在FDA监管范围之外使用。”
然而,缺乏职业道德的公司却可能在新的法案下掠劫无助的患者。医生和制药商可以在法规下逃脱责任。另外,尽管法案规定,制药商向患者提供药物时,只能收取成本费用,但却不要求FDA预审批这些费用。这又会让很多重要的患者权益倡导组织反对这项立法。
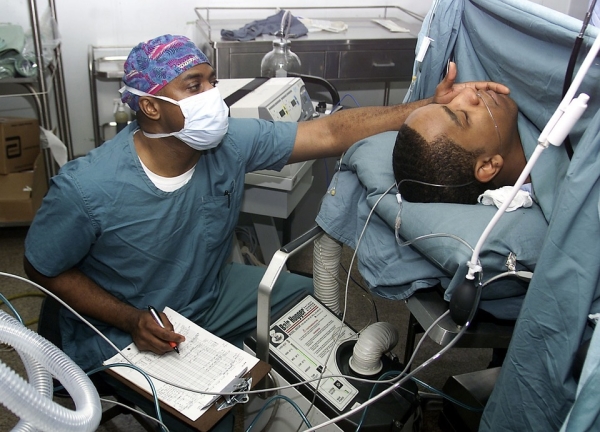
图片来源:pixabay
美国伊利诺伊州的心脏病学家韦伯哈夫·兰加拉詹(Vibhav Rangarajan)曾希望这个法规可以帮他2岁的女儿拉达(Radha)拿到一种试验药物。拉达患有一种名叫异染性脑白质营养不良的罕见病,这种病正破坏她的神经系统。但他认为这个法案对制药公司来说缺乏有意义的激励,“它不会真正改变局面。”
撰文:克劳迪娅·沃利斯(Claudia Wallis)
翻译:贾明月
引进来源:环球科学

本文来自:中国数字科技馆
特别声明:本文转载仅仅是出于科普传播信息的需要,并不意味着代表本网站观点或证实其内容的真实性;如其他媒体、网站或个人从本网站转载使用,须保留本网站注明的“来源”,并自负版权等法律责任;作者如果不希望被转载或其它相关事宜,请与我们接洽。
[责任编辑:环球科学]















 京公网安备11010502039775号
京公网安备11010502039775号





